2 - Procédure d'agrément
2 - Procédure d'agrément sanitaire
2-1 : Composition du dossier d'agrément⚓
De manière générale, il est opportun de s'aider des vade-mecum généraux et sectoriels pour l'instruction des dossiers.
Tableau détaillée des pièces D1 et D2 du dossier d'agrément sanitaire (PDF - 18 pages)
1. Note de présentation de l'établissement⚓
Concept : 1.1. Organisation Générale⚓
Pièces D1 - Transmises à DDecPP
Éléments d'identification de l'entreprise (SIRET / SIREN)
Situation de l'entreprise dans la filière : appartenance à un groupe, à une structure organisée (organisation de producteurs, syndicats, prudhommies...)
Nature et dates d'attribution des précédents agréments le cas échéant
Engagement éventuel dans une démarche qualité, type certification FSSC22000, BRC, IFS ou autre
Présentation synthétique des activités de l'établissement
Pièces D2 - Consultables sur site
Lettre(s) d’attribution des différents agréments
Concept : 1.2. Organigrammes fonctionnels - répartition des personnels⚓
1.2. Organigrammes fonctionnels et répartition des différentes catégories de personnel
Pièces D1 - Transmises à DDecPP :
Organigrammes fonctionnel et hiérarchique non nominatifs
Équipe HACCP : nom, qualité et qualification de la (ou des) personne(s) responsable(s) de la mise au point et du suivi du plan HACCP
2. Description des activités de l'établissement⚓
Concept : 2.1. - Liste des catégories de produits finis⚓
2.1. La liste des catégories de produits finis correspondant à des procédés de fabrication identifiés et leur utilisation prévisible attendue
Pièces D1 - Transmises à DDecPP
Liste des catégories de produits finis correspondant à des procédés de fabrication identifiés et homogènes sur le plan de la maîtrise des dangers, y compris les produits annexes valorisables en alimentation humaine (exemple : arêtes charnues, aponévroses),en précisant, par produit si nécessaire :
composition (matières premières, ingrédients, additifs, allergènes éventuels, etc.),
structure et caractéristiques physico-chimiques (solide, liquide, gel, émulsion, taux d’humidité, pH, activité de l’eau, taux de sel, etc.),
nature du traitement ou de la transformation (chauffage, congélation, dessiccation, salaison, fumaison, etc., et son ampleur),
la présentation finale (degré de manipulation du produit après traitement (ex : tranchage, glaçage,…),
conditionnement et emballage (hermétique, sous vide, sous atmosphère modifiée, etc.) et étiquetage,
conditions de stockage et de distribution, y compris le transport et la manutention,
durée de conservation (par exemple, «date limite de consommation» ou «à consommer de préférence avant le …»),
mode d’emploi,
tout critère microbiologique ou chimique applicable.
l'utilisation prévisible attendue (cuisson avant consommation, consommation en l'état, etc.)
les instructions d'utilisation par le consommateur
le type de liaison (froide ou chaude)
si une catégorie de consommateurs particulière est concernée par certains produits (régimes alimentaires, population sensible,..).
Pour les activités de négoce et/ou de stockage-entreposage (entrepôts) : catégories de produits concernés (conformément aux sections de l'annexe III du règlement (CE) n° 853/2004).
Pièces D2 - Consultables sur site
Éléments de justification (ex. : études de durée de vie, résultats des tests de vieillissement…) par catégorie de produit périssables permettant de justifier la durée de vie.
Concept : Note de vos experts : Études de durée de vie (tests de vieillissement...)⚓
- Ce sont des éléments de justification (ex. : études de durée de vie, résultats des tests de vieillissement...) permettant de valider la durée de vie de différentes catégories de produits périssables.
- La détermination de la durée de vie et sa validation sont très importantes pour la sécurité microbiologique des denrées alimentaires, en particulier pour les aliments prêts à être consommés.
Remarque : Vos Experts VETHYQUA peuvent vous aider...⚓
Nous pouvons vous assister pour la validations de vos durées de vie :
Définir un protocole économique & adapté aux typologies « entreprises-produits ».
Superviser leur mise en œuvre et en tirer les conclusions (adaptation / validation).
Pour plus d'informations sur nos prestations, rendez-vous sur notre site internet !
Concept : 2.2a. - Liste des matières premières et des ingrédients.⚓
2.2. La liste des matières premières ou animaux vivants, des ingrédients
Pièces D1 - Transmises à DDecPP
Lister les matières premières et ingrédients
Pour les entrepôts : sans objet.
Pour les abattoirs : liste des espèces d'animaux abattus.
Concept : 2.2b. - Liste des conditionnements, fournitures et emballages⚓
2.2. La liste des matériaux de conditionnement et d'emballage
Pièces D1 - Transmises à DDecPP
Liste des différents types de conditionnements, d’emballages et autres fournitures utilisés.
On entend par fourniture tout matériel entrant en contact avec des produits (exemples : ficelles, pics à brochettes…).
Pour les entrepôts, sauf en cas d’activité d’emballage : sans objet
Pièces D2 - Consultables sur site
Déclaration de conformité du matériau par rapport à l’utilisation prévue
Concept : Note de vos experts : Certificats d'alimentarité⚓
- Le Paquet Hygiène impose que les conditionnements et emballages des denrées utilisés ne soient pas sources de contamination.
- L'alimentarité correspond à l'aptitude d'un matériel à entrer au contact avec un aliment sans interaction entre eux.
Complément : IMPORTANT = Aptitude au contact avec les aliments⚓
L'aptitude au contact avec les aliments des matériaux est régie par le Règlement CE n°1935/2004 du 27 octobre 2004. Il concerne notamment les emballages et conditionnements.
Ce règlement instaure le principe d'inertie (article 3) :
"Les matériaux et objets doivent être fabriqués conformément aux bonnes pratiques de fabrication afin que, dans les conditions normales ou prévisibles de leur emploi, ils ne cèdent pas aux denrées alimentaires des constituants en une quantité susceptible :
de présenter un danger pour la santé humaine, ou
d'entraîner une modification inacceptable de la composition des denrées ou
une altération des caractères organoleptiques de celles-ci."
Concept : 2.3.a Circuits d'approvisionnement⚓
2.3. La description des circuits d'approvisionnement
Pièces D1 - Transmises à DDecPP
Circuit d’approvisionnement : Provenance des produits : national, UE, pays tiers
Pièces D2 - Consultables sur site
Informations disponibles concernant les fournisseurs
Concept : 2.3.b Circuits de commercialisation⚓
2.3. La description des circuits de commercialisation des produits envisagés
Pièces D1 - Transmises à DDecPP
Circuit de commercialisation envisagé :
Mise sur le marché national, UE ou pays tiers, établissements agréés, de négociants, distribution, restauration sociale (préciser le(s) type(s) d’établissements) ou commerciale.
Pièces D2 - Consultables sur site
Informations disponibles concernant les destinataires.
Concept : 2.4. Les diagrammes de fabrication⚓
Pièces D1 - Transmises à DDecPP
Réaliser un diagramme de fabrication par catégorie de produits homogènes sur le plan de la maîtrise des dangers en indiquant :
toutes les catégories de matières premières, ingrédients et consommables
toutes les étapes de fabrication depuis la réception des matières premières jusqu'à l'expédition des produits finis sans oublier les étapes suivantes : déconditionnement, stockage, préparation des ingrédients, production, attente intermédiaire, recyclage de denrées, conditionnement, emballage, transport...
Préciser les séquences de production et interactions de toutes les étapes sans oublier les reprises et recyclages effectifs de denrées (en interne et des retours).
Il est recommandé de faire apparaître sur le diagramme les locaux de réalisation des différentes étapes et les points déterminants (PRPO, CCP).
Pour les entrepôts, les étapes liées à leur(s) activité(s) sont décrites, telles que : réception, stockage/entreposage, congélation, emballage, préparation de commandes, expédition
Concept : 2.5. Volumes de production⚓
2.5. Les tonnages ou les volumes de production annuels et la capacité journalière maximale
Pièces D1 - Transmises à DDecPP
Tonnages, volume, ou nombre de repas produits annuellement.
Capacité journalière maximale.
Pour les abattoirs : cadences d’abattage.
Sans objet pour les entrepôts.
Concept : 2.6. Gestion des SPAn et déchets⚓
2.6. La liste et les procédures de gestion des sous-produits animaux et des déchets
Pièces D1 - Transmises à DDecPP
Il s’agit de décrire la nature et les destinations des différentes catégories, au sens des règlements (CE) n°183/2005 et (CE) n°1069/2009, de sous-produits animaux générés par l’établissement ainsi que des déchets non alimentaires.
Pour les entrepôts, cela peut concerner, d’une part les déchets non alimentaires, d’autre part les denrées conditionnées/emballées non conformes et retirées de la consommation.
Un tableau peut convenir pour récapituler pour chaque type de déchets :
la nature du déchet,
le lieu de stockage avant enlèvement,
la fréquence d’enlèvement.
Le lieu de stockage peut être matérialisé sur le plan du point 2.9.
Pièces D2 - Consultables sur site
Enregistrement des informations pertinentes
Pour les sous-produits animaux, archivage des documents prévus au règlement (CE) n°1069/2009.
Contrat avec la société d’enlèvement pour les sous-produits de catégorie 1.
Complément : Note de vos experts : Classification en catégories⚓
Le règlement européen (CE) n°1069/2009 classe les sous-produits animaux en trois catégories sur la base de leur risque potentiel pour la santé humaine et animale et l’environnement. Il définit la manière dont les matières de chaque catégorie doivent ou peuvent être éliminées ou valorisées pour certains usages dans le souci de maintenir un niveau élevé de protection de la santé publique et animale. Toutes les matières animales ou d’origine animale (terrestres ou aquatiques), dès lors qu’elles ne sont pas ou plus destinées à l’alimentation humaine, sont par définition concernées par cette réglementation.
Les matières de la catégorie 1
Elles présentent un risque important pour la santé publique (risque d’EST, MRS, risque de présence de substance interdite ou d’un contaminant pour l’environnement, risque sanitaire émergent...). Ces matières doivent être collectées, transportées et identifiées sans retard et sont pour l’essentiel valorisées en biodiesel ou en combustible ou éliminées par incinération, co-incinération ou par mise en décharge après transformation et marquage.
Les matières de la catégorie 2
Elles comprennent les sous-produits animaux présentant un risque moins important pour la santé publique (risque sanitaire classique tel que véhiculé par les animaux trouvés morts en élevage, produits d’origine animale contenant des résidus de médicaments vétérinaires par exemple). Ces produits sont valorisés en vue de certaines utilisations autres que l’alimentation des animaux (engrais organiques, conversion en biogaz, compostage…), y compris sans transformation comme dans le cas du lisier, qui peut être appliqué dans les sols si le contexte sanitaire ne s’y oppose pas. A défaut, ils sont éliminés par incinération, co-incinération ou enfouissement après transformation et marquage.
Les matières de la catégorie 3
Elles présentent un faible risque sanitaire pour la santé animale ou la santé publique et sont les seules qui peuvent être valorisées en alimentation animale. Elles comprennent notamment :
- des parties d’animaux abattus et jugés propres à la consommation humaine mais que la chaîne alimentaire humaine ne valorise pas ou celles provenant d’animaux jugés aptes à l’abattage,
- les denrées alimentaires d’origine animale non destinées à l’alimentation humaine pour des raisons commerciales (« anciennes denrées alimentaires »), dont les matières aquatiques, le lait, les œufs, le miel,...
Seules certaines matières de catégorie 3 peuvent être utilisées dans l’alimentation des animaux, après application d’un traitement approprié dans des installations de transformation agréées. Par ailleurs, au sein des matières de cette catégorie de nombreux produits sont valorisés après des traitements spécifiques pour des usages divers : pharmacie, cosmétique, agronomie (engrais dont compost et digestats de méthanisation), produits manufacturés, produits artisanaux, voire artistiques, énergie.
Concept : 2.7. Volume de stockage⚓
2.7. La capacité de stockage des matières premières, des produits intermédiaires et des produits finis
Pièces D1 - Transmises à DDecPP
A définir pour les matières premières, les produits finis et les produits intermédiaires, et par chambre de stockage :
en froid positif
en froid négatif
à température ambiante
Sous forme de m3 utiles, de nombre de carcasses… selon les denrées.
Prévoir une distinction produits nus / produits emballés.
Pour les entrepôts, la capacité de stockage des produits doit être exprimée en m3
Concept : 2.8. Plan de masse⚓
2.8. Plan de masse, à une échelle lisible, présentant l'ensemble des bâtiments de l'établissement et les éléments de voirie
Pièces D1 - Transmises à DDecPP
Plan de masse présentant :
l'ensemble des bâtiments de l'entreprise et des éléments de voirie,
les aires réservées au nettoyage des véhicules.
Le plan doit être orienté (indication du Nord) et l'échelle précisée
Concept : 2.9. Plan des locaux & équipements⚓
2.9. Un plan d'ensemble de l'établissement, à une échelle lisible, indiquant la disposition des locaux et des équipements
Pièces D1 - Transmises à DDecPP
Plan(s) de l'ensemble des locaux nécessaires au fonctionnement de l'entreprise, indiquant :
la disposition des locaux de travail, d'entreposage et ceux à usage du personnel
l'implantation des divers équipements
L'échelle doit être précisée.
Le ou les plans comportent une schématisation des circuits :
du personnel selon ses fonctions,
des denrées (nues/conditionnées/emballées) de la réception à l’expédition,
des sous-produits animaux et déchets,
des emballages et conditionnements,
du matériel sale vers la zone de lavage et du matériel propre en retour.
Indiquer les secteurs propres et sales, et le cas échéant, les zones très sensibles du point de vue de la sécurité sanitaire des aliments (salle microbiologiquement maîtrisée ou équivalent).
Préciser pour chaque local :
la dénomination et l’utilisation prévue
l’emplacement :
des équipements fixes ou mobiles,
des dispositifs de lavage installés : lave-mains, stérilisateurs à couteaux, centrales de nettoyage,…
des dispositifs de cuisson, pasteurisation, stérilisation et leurs moyens de contrôle (exemples : stérilisateurs, fours, autoclaves),
du matériel utilisé pour la transformation des produits (ex : poussoirs, embossoirs, cutters, malaxeurs),
des dispositifs de ventilation, aération, extraction de buées, zones de surpression, plafonds filtrants,
des dispositifs de production de glace,
du matériel utilisé pour le stockage intermédiaire des denrées,
des dispositifs d’évacuation des eaux résiduaires
Visualiser sur le plan la zone de stockage du matériel mobile
Le plan de masse et le plan de l’établissement peuvent être communs sous réserve de lisibilité.
Les plans manuscrits peuvent être acceptés.
Pièces D2 - Consultables sur site
Mise à jour des plans lors de modifications – pour les modifications de process et de locaux, se reporter au chapitre 3 de la présente instruction
Concept : 2.10. Conditions de fonctionnement⚓
2.10. La description des conditions de fonctionnement
Pièces D1 - Transmises à DDecPP
Préciser les obligations liées à la planification du travail :
Horaires de travail (y compris les horaires réservés au nettoyagedésinfection), pauses, jours et périodes de fermeture,
Effectifs : nombre de personnes par secteur d'activité, nombre d'équipes et fréquence de rotation, emplois saisonniers ou temporaires,
Activité à caractère saisonnier ou non.
3. Le Plan de Maîtrise Sanitaire⚓
3.1. Les documents relatifs aux Bonnes Pratiques d'Hygiène⚓
Concept : 3.1.1a. Personnel - Plan de formation⚓
Plan de formation (initiale et continue)
Pièces D1 - Transmises à DDecPP
Objectifs et contenu général
Catégories de personnel concernées
Cas particulier des abattoirs inclure : formation à la protection animale + formation au retrait des produits
Pièces D2 - Consultables sur site
Procédure de qualification avant embauche (par exemple : remise d’un livret d’accueil).
Détail des modules de formation continue.
Qualité du (des) formateur(s) : interne à l’établissement ou société extérieure (contrat éventuel).
Liste et fonction des personnes ayant suivi la formation.
Attestations de présence visées par les agents.
Attestation de formation du responsable de sa mise en œuvre à la méthodeHACCP ou à l’utilisation du GBPH validé.
Vérification par l’exploitant de l’effectivité et de l’efficacité de la formation
Concept : 3.1.1b. Personnel - Tenue vestimentaire⚓
Pièces D1 - Transmises à DDecPP
Description de l'équipement vestimentaire du personnel.
Préciser les tenues à disposition du personnel et les modalités d'entretien (interne à l'entreprise ou prestataire)
Pièces D2 - Consultables sur site
Modalités de gestion des tenues vestimentaires :
les conditions de stockage des tenues propres, « en cours » et des vêtements de ville (vestiaire individuel, cloisonné ou pas…),
qui est responsable de l’entretien des tenues : les employés, l’entreprise, un prestataire (présentation du contrat).
Concept : 3.1.1c. Personnel - État de santé⚓
Pièces D1 - Transmises à DDecPP
Liste des instructions
Pièces D2 - Consultables sur site
Registre des instructions
Concept : 3.1.2 - Maintenance locaux / équipements / matériel⚓
3.1.2. L'organisation de la maintenance des locaux, des équipements et du matériel
Pièces D1 - Transmises à DDecPP
Description générale de la maintenance :
Liste des locaux, équipements et matériels concernés
Préciser l'organisation (interne à l'entreprise ou prestataire(s))
Pièces D2 - Consultables sur site
Description détaillée des modalités de maintenance préventive et curative des locaux, équipements et matériels : quoi, qui, comment, à quelle fréquence, contrats de maintenance ? Modalités de suivi.
Modalités de vérification de la maintenance
Enregistrements des opérations de maintenance réalisées : comptes rendus de passage et actions correctives le cas échéant.
Concept : 3.1.3a - Plan de nettoyage - désinfection (PND)⚓
3.1.3. Mesures d'hygiène préconisées avant, pendant et après la production
Pièces D1 - Transmises à DDecPP
Plan de nettoyage - désinfection (PND) et plan de contrôle de son efficacité
Organisation (interne à l'entreprise ou prestataire(s))
Plan de nettoyage-désinfection :
Pour chaque local et matériel, indiquer la méthode appliquée, sa fréquence, les modalités d'enregistrement de sa réalisation, la procédure de gestion des nonconformités (actions correctives),
modèle de support d'enregistrement de la réalisation du nettoyage-désinfection,
Plan de contrôle de l'efficacité du nettoyage :
Décrire comment est vérifiée l'efficacité du PND (visuel, ATPmétrie, lames de surface...) sur les surfaces et équipements et du matériel en contact avec les denrées alimentaires (plans de travail, couteaux, plateaux...).
Préciser à quel moment est effectuée la vérification (avant ou après la production),
Procédure de gestion des non-conformités (actions correctives).
Modèle de support d'enregistrement des contrôles et des actions correctives.
Pièces D2 - Consultables sur site
Dans le cas d’une société prestataire, présenter la copie du contrat
Fiches techniques des produits utilisés ou étiquettes si elles comportent les indications nécessaires (usage, mode d’utilisation, dosage,…).
Enregistrements au minimum des nettoyages non quotidiens (ex : évaporateurs en atelier de boucherie).
Enregistrements des contrôles, résultats et actions correctives le cas échéant de la surveillance visuelle et/ou microbiologique.
Concept : 3.1.3b - Hygiène des manipulations⚓
3.1.3. Mesures d'hygiène préconisées avant, pendant et après la production
Pièces D1 - Transmises à DDecPP
Instructions de travail relatives à l'hygiène des manipulations
Liste des instructions
Pièces D2 - Consultables sur site
Descriptions des instructions prévues en matière d’hygiène des manipulations :
instructions générales ou détaillées dans les fiches de poste.
Par exemple, et lorsque l'analyse des dangers le justifie :
AVANT LA PRODUCTION :
Vérification de la propreté des locaux et du matériel,
Vérification de la température des locaux et des stérilisateurs à couteaux,
Vérification du bon fonctionnement des lave-mains et stérilisateurs à couteaux,
Vérification de l’approvisionnement en produits et en consommables des différents postes de lavage/nettoyage des mains et du petit matériel.
PENDANT LA PRODUCTION :
Modalités d’accès à certaines zones de l’établissement (salle blanche, bouverie en abattoir…),
Propreté du personnel et du matériel,
Maintien de propreté des équipements,
Précautions prises lors des manipulations,
Approvisionnement en produits et en consommables des différents postes de lavage/nettoyage des mains et du petit matériel.
APRÈS LA PRODUCTION :
Circulation des agents dans les ateliers.
Concept : 3.1.4 - Plan de lutte contre les nuisibles⚓
Pièces D1 - Transmises à DDecPP
Plan avec légende de l'établissement où figurent les emplacements numérotés des dispositifs de lutte (ces repères doivent se retrouver dans l'établissement et ses abords).
Le plan peut être commun avec le plan de l'établissement prévu au point 2.9 sous réserve de lisibilité.
Préciser les types de nuisibles concernés.
Préciser l'organisation (interne à l'entreprise ou prestataire(s)).
En cas d'organisation interne :
Protocole interne à l'établissement, en précisant la fréquence et la nature des contrôles
Modèle des fiches de contrôle utilisées
Procédure de gestion des non-conformités (actions correctives)
Procédure de vérification
Pièces D2 - Consultables sur site
Fiches techniques des produits employés
En cas de recours à un prestataire :
contrat de lutte contre les nuisibles,
classement chronologique des rapports de visite détaillés.
En cas d’organisation interne : enregistrements des contrôles.
Actions correctives mises en œuvre en cas d'anomalies.
Concept : 3.1.5 - Eau potable / Eaux résiduaires⚓
3.1.5. L'approvisionnement en eau, les circuits d'arrivée d'eau potable/eau de mer et d'évacuation des eaux résiduaires
Sans objet pour les entrepôts
Pièces D1 - Transmises à DDecPP
Plan de l'établissement à une échelle lisible, faisant apparaître :
les points d'eau numérotés,
la description d'un éventuel dispositif de traitement de l'eau,
les réseaux de distribution de l'eau potable/eau de mer et d'évacuation des eaux résiduaires.
Ce descriptif peut être réalisé sur le plan d'ensemble cité au point 2.9.
RÉSEAU PUBLIC :
Attestation de potabilité de l'eau ou attestation de raccordement de l'établissement au réseau public (à défaut facture d'eau).
Adjoindre une déclaration relative à la non-utilisation d'eau d'une autre origine en dehors des utilisations possibles prévues réglementairement.
RESSOURCE PRIVÉE :
Copie de l'arrêté préfectoral autorisant l'utilisation de l'eau d'une autre origine avec éventuellement le résultat des analyses effectuées.
Dispositifs de contrôle mis en place pour assurer et contrôler la potabilité de l'eau au sein de l'établissement.
Dans le cas particulier des produits de la pêche, décrire les conditions d'utilisation de l'eau propre au sens du Règlement (CE) n°852/2004
Procédure de gestion des non-conformités (actions correctives)
Pièces D2 - Consultables sur site
Relevés des compteurs, factures d'eau le cas échéant, ou autre moyen d'évaluer les consommations (notamment s'il existe plusieurs provenances).
Description des différentes interventions sur le réseau de distribution d'eau (réparation, changement de réseaux de distribution d'eau...).
Résultats des analyses bactériologiques et chimiques portant sur l'eau en contact direct ou indirect avec les denrées (dont la glace alimentaire).
Les résultats d'analyse font référence au numéro du point de prélèvement (de préférence en fin de réseau).
Traitements effectués sur l'eau à l'intérieur de l'entreprise et vérification de leur efficacité. Description des dispositifs tels que adoucisseurs, javellisation, ionisation...
Recyclage de l'eau : conditions de stockage, d'emploi et de contrôle
Actions correctives en cas de non-conformité et enregistrements correspondants
Concept : 3.1.6 - La maîtrise des températures⚓
Pièces D1 - Transmises à DDecPP
Lister les locaux sous température dirigée en précisant les températures recherchées (cela peut fait sur le plan sous 2.9.) et les températures à ne pas dépasser.
Décrire le système et le matériel de surveillance des températures (locaux, denrées), les modalités d'enregistrement et d'alertes en cas d'anomalies et les mesures correctives (produit / procédé).
Modèle de support d'enregistrement des contrôles.
Pièces D2 - Consultables sur site
Enregistrements des contrôles et des actions correctives (produits, procédés).
Concept : 3.1.7 - Réception & Expédition⚓
3.1.7. Le contrôle à réception et à expédition.
Pièces D1 - Transmises à DDecPP
CONTRÔLES A RÉCEPTION (HORS CCP)
Pour les catégories de produits reçus de l'extérieur entrant en contact avec les denrées ou utilisés dans leur fabrication (matières premières, ingrédients, matériaux de conditionnement et d'emballage, et produits finis) :
Protocole formalisé de contrôle à réception des produits dont la réception n'est pas considérée comme un CCP : fréquence du contrôle, points de contrôle ;
Modèle de support d'enregistrement des contrôles ou description des modalités d'enregistrement ;
Procédure de gestion des non-conformités (critères de refus, actions correctives).
CONTRÔLES AVANT EXPÉDITION DES PRODUITS FINIS :
Procédure de contrôle des produits avant expédition.
Pièces D2 - Consultables sur site
Instructions de travail relatives au contrôle des matières premières, mentionnant en particulier les critères de refus ou de déclassement des denrées reçues.
Le cas échéant, modes opératoires associés (par exemple modalités de prise de température).
Enregistrements des contrôles à réception et des actions correctives,
S'ils sont prévus, enregistrement des contrôles avant expédition
3.2. Documents relatifs aux procédures fondées sur l'HACCP⚓
Concept : 3.2.1. Le champ d'application de l'étude⚓
Liste des différents plans HACCP « Produits/procédés de fabrication » homogènes sur le plan de la maîtrise des dangers, sans oublier les activités annexes (ex : négoce).
Préciser les étapes de début et de fin
Concept : 3.2.2. L’analyse des dangers⚓
Les documents relatifs à l’analyse des dangers biologiques, chimiques et physiques et mesures de maîtrise associées (principe 1)
Pièces D1 - Transmises à DDecPP
1 - Identifier, pour chaque ingrédient ou matériau reçu de l’extérieur, et pour chaque étape de la transformation, les dangers raisonnablement attendus parmi :
les dangers biologiques : organismes pathogènes, parasites, toxines...
les dangers chimiques : résidus de nettoyage, substances toxiques utilisées dans l’entreprise, résidus de médicaments et contaminants de l’environnement, allergènes…
les dangers physiques : corps étrangers, insectes, radionucléïdes,..
Justifier les choix retenus (lister les sources de justification).
A chaque étape, préciser la condition (PIXS) et la cause (5M) d’apparition du danger
Rappeler le niveau acceptable de danger pour le produit fini : au minimum niveau réglementaire lorsqu’il existe.
2 - Hiérarchiser les dangers à l’aide d’un système de cotation (gravité x probabilité) ou d’une évaluation par jugement professionnel pour aboutir à une liste de dangers significatifs (pour lesquels la maîtrise est essentielle à la production d’un aliment sûr)
3 - Décrire les mesures de maîtrise associées à chaque danger retenu (ou groupe de dangers pour les mesures de maîtrise identiques).
Les dispositions précédentes peuvent être présentées sous forme d’un tableau établi étape par étape du diagramme de fabrication (cf. tableau ci-après de l’analyse des dangers).
Pièces D2 - Consultables sur site
Détail des sources de justification outils disponibles (ANSES, EFSA, Réglementation, GBPH...) ; retours, plaintes...
Instructions précisant, si nécessaire, les modalités d’application des mesures de maîtrise
Enregistrement des mesures de maîtrise.
3.2.2. Analyse des dangers biologiques, chimiques et physiques et mesures de maîtrise⚓
3.2.2. Les documents relatifs à l'analyse des dangers biologiques, chimiques et physiques et mesures de maîtrise associées (principe n° 1).
Concept : 3.2.3a CCP et PRPO - Identification⚓
Identifier les points déterminants (Principe 2)
Pièces D1 - Transmises à DDecPP
Pour chaque danger significatif identifié, lister les CCP et les PRPO retenus en les numérotant.
Justifier les décisions relatives au choix de ces points déterminants ou justifier l’absence de point déterminant le cas échéant. (arbre de décision ou jugement professionnel)
En l’absence de point déterminant, les principes 3, 4 et 5 sont sans objet.
Concept : 3.2.3b - CCP-PRPO - Limites critiques⚓
Définir les limites critiques pour les CCP et les objectifs/niveaux seuils de maîtrise pour les PRPO (Principe 3)
Pièces D1 - Transmises à DDecPP
Définir des limites critiques pour chaque CCP (et, le cas échéant, les valeurs cibles) ainsi que les niveaux des seuils de maîtrise pour les PRPO.
Établir la liste des documents de validation des mesures de maîtrise, justifiant le choix des limites critiques et des valeurs cibles éventuelles pour les CCP, ainsi que les niveaux des seuils de maîtrise pour les PRPO.
Pièces D2 - Consultables sur site
Documentation justifiant le choix des limites critiques et des valeurs cibles éventuelles ;
Documents liés à la validation des mesures de maîtrise
Complément : Modèles documentaires VETHYQUA⚓
PrPo | Objectif / Niveau seuil de maîtrise | Procédure de surveillance (référence du document) | Actions correctives/Corrections (référence du document) | Enregistrement (référence du document) |
|---|---|---|---|---|
PrPo n°01 |
CCP | Limite critique | Procédure de surveillance (référence du document) | Actions correctives/Corrections (référence du document) | Enregistrement (référence du document) |
|---|---|---|---|---|
CCP n°01 |
Concept : 3.2.3b - CCP-PRPO - Surveillance⚓
Procédures de surveillance des points déterminants (Principe 4)
Pièces D1 - Transmises à DDecPP
Pour chaque CCP et PRPO, décrire les modalités de surveillance des critères retenus :
Qui (personnels de surveillance et leurs remplaçants) ?
Quoi ?
Où ?
Quand (la fréquence de la surveillance doit être compatible avec une action corrective sur le produit) ?
Comment ?
Modèle de support d’enregistrement.
Pièces D2 - Consultables sur site
Pour chaque point déterminant :
Instruction précisant la méthode de surveillance, le cas échéant
Enregistrement des opérations de surveillance
Concept : 3.2.3b - CCP-PRPO - Actions correctives et corrections⚓
Actions correctives et corrections pour les points déterminants (dont PRPO et CCP) (Principe 5)
Pièces D1 - Transmises à DDecPP
Procédure écrite définissant :
1 - les actions correctives, incluant 3 types de mesures :
la recherche des causes du dysfonctionnement constaté ;
l’assurance du retour à la maîtrise ;
les mesures permettant d’éviter le renouvellement du dysfonctionnement (action corrective sur le procédé).
2 - Les corrections : devenir des denrées concernées par le dysfonctionnement, obligatoire pour les CCP et facultatif (à analyser au cas par cas) pour les PRPO.
Modèle de support d’enregistrement.
Pièces D2 - Consultables sur site
Instructions définissant la mise en œuvre des actions correctives (comprenant la description de la non-conformité, l’analyse des causes, les mesures appliquées au procédé, les mesures permettant d’éviter la répétition de l’anomalie) et des corrections (mesures appliquées au produit).
Enregistrements des actions correctives à chaque dépassement de limite critique (pour les CCP) ou de niveau seuil de maîtrise (pour les PRPO), apportant la preuve de leur application.
Enregistrements des corrections effectuées à chaque dépassement de limite critique (pour les CCP) et enregistrements des corrections effectuées (lorsqu’il y en a) lors des pertes de maîtrise des PRPO.
Concept : 3.2.4 Vérification⚓
Les documents relatifs à la vérification (Principe 6)
Pièces D1 - Transmises à DDecPP
Procédures de vérification du PMS :
De la mise en œuvre effective du PMS : modalités pratiques (suivi des enregistrements, audits, revues de direction) et conséquences (mise à jour du plan HACCP…)
De l'efficacité du PMS :
plan d'auto-contrôles analytiques
analyses des réclamations-clients
modalités de contrôle de mesures de maîtrise : celles-ci peuvent éventuellement être décrites dans les mesures de maîtrise correspondantes.
Pièces D2 - Consultables sur site
Enregistrements de la vérification de la bonne application des procédures de surveillance, des BPH, des mesures de maîtrise et des enregistrements associés : audits internes, audits externes, revues de direction.
Résultats des auto-contrôles analytiques et exploitation.
Concept : Contrat avec le laboratoire d'analyses microbiologiques ⚓
Présenter le(s) contrat(s) reprenant le descriptif des analyses mises en place :
analyses microbiologiques des denrées (pour validation de durée de vie, analyses de routine...),
analyse microbiologique et chimique de l'eau,
prélèvements de surface.
Le contrat reprend :
le nombre d'analyses,
la fréquence de analyses,
les micro-organismes recherchés par catégorie de produits.
3.3. Procédures de traçabilité et de gestion des produits non-conformes⚓
Concept : 3.3. Traçabilité - Gestion des Produits NC⚓
Les procédures de traçabilité et de gestion des produits non conformes (retrait, rappel…)
Pièces D1 - Transmises à DDecPP
Description du système de traçabilité
Procédure relative à la gestion des produits non conformes
Procédure permettant la mise en œuvre d’un retrait/rappel en cas de défaut identifié.
Pièces D2 - Consultables sur site
Éléments relatifs à la traçabilité qualitative et quantitative (supports papiers ou informatiques).
Enregistrements relatifs à la gestion des produits non conformes (matières premières ou produits finis).
3.4 : Les documents relatifs à la protection des animaux à l'abattoir⚓
Concept : 3.4 - Protection des animaux à l'abattoir⚓
Les documents relatifs à la protection des animaux à l'abattoir
Pièces D1 - Transmises à DDecPP
Description des modes opératoires normalisés (MON) à toutes les étapes du déchargement des animaux jusqu'aux premières étapes d'habillage et pour toutes les espèces et catégories d'animaux et comprenant notamment :
le déchargement, l’observation des animaux, l’examen des informations de la
chaîne alimentaire (ICA) et les critères du premier tri des animaux;
l’hébergement et les manipulations;
l’immobilisation;
l’étourdissement et le contrôle de son efficacité;
la mise à mort;
la gestion des animaux à problèmes.
Les MON doivent décrire le fonctionnement réel de l'établissement. Pour chaque étape, chaque espèce et chaque catégorie d'animaux, les points suivants doivent être précisés :
la description du fonctionnement normal de l'établissement. Les éléments permettant de garantir le respect des exigences réglementaires à chacune des étapes et pour toutes les espèces et catégories d'animaux doivent être apportés ;
les modalités du contrôle interne conformément aux dispositions du règlement (CE) n°1099/2009 et comprenant les modalités de surveillance et de vérification du respect des exigences réglementaires relatives à la protection animale, de la bonne application et de l'efficacité des procédures en place ; Qui, Quoi, Quand, Où, Comment, A quelle fréquence ?
les anomalies envisageables à partir de critères mesurables ou observables identifiés ;
les actions correctives prévues pour y remédier ;
les modèles de support d'enregistrement des contrôles et du suivi des nonconformités
Pièces D2 - Consultables sur site
La documentation justifiant le choix des modalités de surveillance et de vérification.
Le registre RPA dûment complété.
Les enregistrements des contrôles réalisés en matière de surveillance et de vérification ainsi que les actions correctives mises en oeuvre en cas d'anomalies
Les résultats des audits relatifs à la protection animale (audits internes ou externes)
La revue du bilan du contrôle interne par l'équipe dirigeante comprenant le suivi des nonconformités par la recherche des causes du dysfonctionnement constaté, l’assurance du retour à la maîtrise et les mesures permettant d’éviter le renouvellement du dysfonctionnement en vue d'une amélioration continue de la protection animale.
Les instructions mises à disposition du personnel.
2.2. Procédure d’agrément - La demande d’agrément sanitaire⚓
Procédure | 1 – Envoi par le professionnel | 2 – Réception de la demande : Accusé d’enregistrement | 3 – Envoi de l’accusé de réception de la demande (en précisant éventuellement les pièces manquantes.) |
Électronique | CERFA 13983 en ligne | Récépissé envoyé automatiquementau demandeur  | Délai de 10 jours1 à compter de l’envoi du récépissé. Vérification que toutes les pièces du dossier sont présentes (pas d’analyse de fond, uniquement présence ou absence) Le délai de deux mois commence à partir de la date de réception de la demande |
Papier | CERFA 13983 | Récépissé papier à renvoyer au demandeur  | Délai raisonnable à compter de l’envoi du récépissé : 10 jours. Vérification que toutes les pièces du dossier sont présentes (pas d’analyse de fond, uniquement présence ou absence) Le délai de deux mois commence à partir de la date de réception de la demande |
Conseil :
1 Article R.112-11-2 du Code des relations entre le public et l'administration
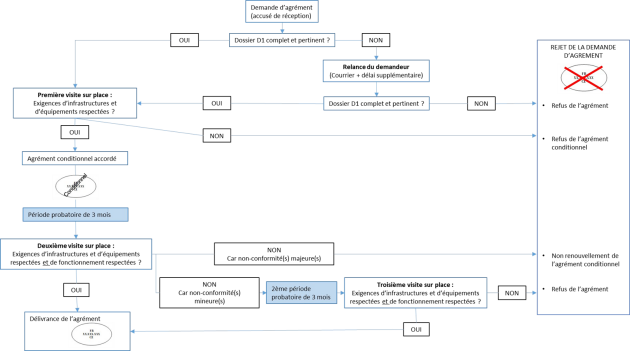
2.3. Procédure d’agrément complète⚓
2.4. Exemples de procédures d’agrément – Décision implicite de refus⚓
Cas 1 : dossier complet + silence de la DDecPP⚓
Cas 2 : dossier complet + décision de la DDecPP⚓
1 juin | 7 juin |
| 12 juillet |
| 12 septembre |
Date de réception | Accusé de réception indiquant comme date de réception le 01 juin |
| Décision d’accorder ou non l’agrément | Délai de recours : contestation de la décision possible par recours gracieux (2 mois) à partir de la date de réception par le demandeur | Fin du délai de recours gracieux |
Cas 3 : dossier incomplet + pas d’envoi de pièces complémentaires + silence de la DDecPP⚓
1 juin | 7 juin | 12 juillet | 12 août | 1 septembre |
| 1 novembre |
Date de réception | Accusé de réception indiquant comme date de réception le 01 juin | Dossier incomplet : DDecPP donne un délai pour fournir les pièces complémentaires SUSPENSION DU DELAI DE 2 MOIS POUR LA DUREE DU DELAI SUPPLEMENTAIRE (Exemple : 1 mois) | Fin du délai supplémentaire fixé par la DDecPP. Pièces complémentaires non reçues. Reprise du délai | Fin du délai : Décision implicite de refus (2 mois + 1 mois supplémentaire) | Délai de recours : contestation de la décision possible par recours gracieux (2 mois) | Fin du délai de recours gracieux |
Cas 4 : dossier incomplet + envoi de pièces complémentaires + silence de la DDecPP⚓
1 juin | 7 juin | 1 juillet | 20 juillet | 20 août |
| 20 octobre |
Date de réception | Accusé de réception indiquant comme date de réception le 01 juin | Dossier incomplet : DDecPP donne un délai pour fournir les pièces complémentaires SUSPENSION DU DELAI DE 2 MOIS POUR LA DUREE DU DELAI SUPPLEMENTAIRE | Réception des pièces complémentaires Reprise du délai à compter de date de réception | Fin du délai Décision implicite de refus (2 mois + 20 jours) | Délai de recours : contestation de la décision possible par recours gracieux (2 mois) | Fin du délai de recours gracieux |
Article L215-5 du Code des relations entre le public et l'administration : « Lorsqu’une demande adressée à l’administration est incomplète, celle-ci indique au demandeur les pièces et informations manquantes (...). Elle fixe un délai pour la réception de ces pièces et informations. Le délai au terme duquel, à défaut de décision expresse, la demande est réputée rejetée est suspendu pendant le délai imparti pour produire les pièces et informations requises. Toutefois, la production de ces pièces et informations avant l’expiration du délai fixé met fin à cette suspension. »
Cas 5 : dossier adressé à une administration incompétente⚓
1 juin | 10 juin | 11 juin | 20 juin |
| 1 août |
| 1 octobre |
Date de réception | Préfecture envoie le dossier à la DDecPP et prévient l’administré | Réception du dossier à la DDecPP | Accusé de réception indiquant comme date de réception le 01 juin |
| Décision implicite de refus (2 mois) | Délai de recours : contestation de la décision possible par recours gracieux (2 mois) | Fin du délai de recours gracieux |
NB : l’accusé de réception doit également indiquer la date à laquelle la décision de rejet va naître [date de réception + 2 mois]
Conseil :
[1] Renvoi automatique ou courrier, selon la procédure choisie, du récépissé de demande.
[2] Dans un délai de 7 jours suivant la réception du dossier par voie électronique, par cohérence, 7 jours pour les demandes postales.
[3] Une décision de refus ou de rejet de la demande d’agrément ne peut faire l’objet d’un recours contentieux auprès du tribunal administratif qu’après rejet d’un recours gracieux préalable à l’encontre de l’auteur de la décision (Préfet dans le cas de l’agrément sanitaire).
[4] /26