1 - Validation DVM
1. Détermination, validation de la durée de vie microbiologique
1.1 Description du produit et du procédé et classement en catégories de produits finis homogènes⚓
Il s'agit de la première étape du processus de détermination d'une DVM. Cela constitue un pré-requis obligatoire.
a) Identification et description de l'aliment
Pour chaque aliment ou type d'aliment, il convient d'identifier la nature du produit, les dénominations, formats, poids, matières premières et ingrédients (y compris additifs), conditionnements, température de conservation mentionnée sur l'étiquetage ou toute autre forme d'identification qui intègre ces éléments. Cette description doit prendre en compte les conséquences éventuelles des associations de ces paramètres.
La description comprend les informations relatives aux caractéristiques physico-chimiques et biologiques ayant une influence sur la DVM de l'aliment concerné, par exemple, pH, acides organiques, aw, teneur en sel/sucres, quantification de la flore technologique et/ou naturelle, concentration en additifs utilisés (surtout conservateurs), etc. Il convient d'identifier les plages raisonnablement prévisibles de variation et les données doivent être représentatives de la variabilité des produits concernés. Pour les produits d'assemblage (tel que les sandwichs), il est nécessaire de mesurer les caractéristiques physico-chimiques et/ou microbiologique pour chaque composant.
Si les caractéristiques physico-chimiques et biologiques sont susceptibles d'évoluer au cours de la durée de vie, des éléments relatifs aux cinétiques d'évolution doivent être disponibles. Pour certains produits et procédés, le niveau maximal de contamination ne se situe pas en fin de durée de vie, mais à un stade antérieur qu'il convient d'identifier au cours de la durée de vie du produit.
b) Description du procédé de fabrication et des conditions de distribution
Une description détaillée du procédé de fabrication et de distribution doit être disponible (formulation, préparation, transformation, conditionnement, stockage, transport, distribution) en prenant en compte les paramètres les plus défavorables d'un point de vue sanitaire susceptibles d'être appliqués (exemples : délai de mise en œuvre des matières premières, prise en compte des durées de stockage intermédiaire éventuel, etc.). Le cas échéant, il convient de préciser les caractéristiques du procédé qui ont un impact sur la DVM.
Une attention particulière doit être portée sur les conditions de stockage, de transport et de distribution des denrées alimentaires très périssables concernées par une DLC :
type de conditionnement, atmosphère de conditionnement (air, sous-vide, atmosphère modifiée),
si conditionnement sous atmosphère modifiée, composition du mélange gazeux,
température et durée de conservation définies par le fabricant ou réglementées, ainsi que plages de variation possibles, circuit de distribution du produit s'il est connu.
Il sera porté une attention particulière à la définition de la date d'origine Je à partir de laquelle est déterminée la DVM ; cette date correspond à l'étape la plus appropriée et pertinente de la fabrication ; pour un aliment donné, elle est toujours la même.
Les conditions d'utilisation raisonnablement prévisibles par le consommateur sont répertoriées, notamment les mentions figurant sur l'étiquetage du produit (conditions de conservation après ouverture, traitement du produit conseillé pour la consommation du produit par exemple).
c) Classement des produits en catégories de produits finis homogènes
En fonction des éléments décrits précédemment, les exploitants doivent classer Ieurs produits en catégories de produits finis homogènes sur le plan de la maîtrise des dangers microbiologiques.
L'évaluation des données doit porter sur un procédé de fabrication stabilisé. La variabilité des caractéristiques physico-chimiques et microbiologiques intra-lot (au sein d'un même lot) et inter-lots (entre différents lots de production) doit être connue et maîtrisée, notamment les valeurs les plus défavorables d'un point de vue sanitaire. Dans le cas d'une hétérogénéité de ces caractéristiques au sein d'une catégorie de produits, l'exploitant redéfinit de nouvelles catégories de produits. Le cas échéant, les Instituts Agro- industriels (ITAI), membres du RMT Actia Qualima 10 peuvent fournir un appui dans la mise en œuvre de cette démarche.
Conseil :
10 AERIAL, ACTALIA, ADIV, ADRIA, CTCPA, IFIP
1.3 Littérature scientifique, bibliographie ou études antérieures⚓
Un large éventail de données est disponible dans les revues scientifiques (ouvrages, journaux, avis), les logiciels de microbiologie prévisionnelle ou auprès des Instituts Techniques Agro-Industriels (ITAI) et des centres techniques.
Quand un opérateur a établi les caractéristiques physico-chimiques d'un produit (pH, a notamment), ainsi que les conditions dans lesquelles il est fabriqué, conditionné et stocké (température de conservation, type de conditionnement, DLC), ces informations peuvent être utilisées pour comparer, pour le produit en question, les données existantes dans la littérature technique et scientifique sur la survie et la croissance des micro-organismes d'intérêt, sans oublier de tenir compte de la variabilité inhérente au produit et au procédé.
Des études menées sur des modèles aliments, et/ou des produits similaires ou présentant des similitudes quant à certaines caractéristiques ayant une influence sur la DVM de l'aliment, peuvent également fournir des informations utiles. Des éléments précis doivent être disponibles, relatifs notamment à la description de l'aliment et aux conditions de conservation pour permettre de justifier l'utilisation des résultats de ces études, et expliciter comment les données ont été exploitées et adaptées au produit et au site considérés (cf.partie II.3-de la présente instruction).
1.4 - Tests de vieillissement⚓
Les tests de vieillissement [11] permettent d'évaluer la croissance des micro-organismes dans les aliments naturellement contaminés, conservés dans des conditions raisonnablement prévisibles. La température et la durée de conservation sont des paramètres essentiels agissant sur le développement microbien. Les tests de vieillissement incluent donc une rupture de la chaîne du froid, sauf si le professionnel peut justifier d'une chaîne du froid totalement maîtrisée.
Ces tests, faciles à mettre en œuvre, sont incontournables et fournissent des informations essentielles et suffisantes pour valider et vérifier la durée de vie microbiologique au regard des flores normalement présentes dans un aliment (flores indicatrices d'hygiène et micro-organismes d'altération). Les tests de vieillissement correspondent à des analyses réalisés en fin de production ou début de DVM (au plus proche du J0) et en fin de DVM.
En revanche, dans le cadre des tests de vieillissement, la recherche des micro-organismes pathogènes à faible prévalence (critères de sécurité ou autres) soumis à un critère qualitatif (absence dans x grammes) n'est pas pertinente pour la validation d'une DVM : il en est de même pour la démarche de vérification de la DVM qui abordée dans le § suivant. La recherche de ces micro-organismes pathogènes doit, en revanche, être réalisée dans le cadre des auto-contrôles à J0 dans l'objectif d'évaluer le niveau de maîtrise du procédé de fabrication et de pouvoir mettre en œuvre sans délai des mesures de gestion en cas de résultat non-conforme. Pour les pathogènes, il s'agit d'analyse de surveillance et non de validation de non croissance des pathogènes.
Les lignes directrices pour la mise en œuvre des tests de vieillissement sont décrites dans la norme NF V01-003 [12] et, pour Listeria monocytogenes dans les denrées prêtes à consommer, dans le chapitre 4 du guide technique du Laboratoire de référence de l'Union européenne [13] pour Listeria monocytogenes.
Pour la validation initiale d'une DVM, les tests de vieillissement doivent porter sur tous les microorganismes identifiés dans l'analyse des dangers pour lesquels il existe un critère quantitatif en fin de DVM (critères réglementaires, critères définis dans les GBPH validés, critères des interprofessions...). Le cas particulier de Listeria monocytogenes est traité à part (cf. paragraphe II.b.3). Les tests de vieillissement sont réalisés par un laboratoire satisfaisant aux exigences générales concernant la compétence des laboratoires (de préférence par des laboratoires accrédités ou, a minima sous assurance qualité et reliés à un réseau d'analyses d'inter-comparaison) et mettant en œuvre les méthodes d'analyse de référence précisées en annexe I du Reg CE 2073/2005 ou les méthodes alternatives commerciales validées par rapport à la méthode de référence et certifiées par une tierce partie conformément au protocole défini dans la norme NF EN ISO 16140 (2003) ou la norme NF EN ISO 16140-2 (2016).
Ces analyses sont réalisées sur au moins un produit représentatif de chaque catégorie de produits finis correspondant à un procédé de fabrication identifié et homogène sur le plan de la maîtrise des dangers microbiologiques et selon un plan d'échantillonnage représentatif des conditions de production avec, au minimum, n=5, en application du Reg CE 2073/2005.
Il peut s'agir de cinq unités :
- issues du même lot : afin de tenir compte de la variabilité inter-lots, il est recommandé de renouveler ces analyses, de préférence pour trois lots de fabrication ;
- ou, pour les petites structures, issues de cinq lots différents (à raison d'une unité par lot) d'un même produit représentatif de la catégorie de produits finis homogènes, afin de prendre en compte la variabilité inter-lots.
La manière dont ces échantillons sont sélectionnés aura un impact sur la fiabilité du résultat. Si plusieurs prélèvements sont réalisés au cours de la fabrication d'un lot, il devront être représentatifs des différentes étapes de cette séquence :
- le début de la production peut être marqué par une montée en température insuffisante des équipements, par une contamination liée à l'introduction des ingrédients, ...
- la fin de la production peut être associée à une succession d'ouvertures/fermetures d'un équipement, avec autant de risques de contamination,
- plus généralement, les différents échantillons doivent permettre d'illustrer la diversité susceptible d'exister dans la qualité du lot fabriqué ; si cette diversité est très importante, il convient de revenir en arrière et de s'interroger sur la segmentation de la production en lots.
Si un seul échantillon est sélectionné, celui-ci doit illustrer les conditions de fabrication les plus défavorables, c'est-à-dire les plus risquées au regard d'une possible contamination du produit. Le choix de cet échantillon doit donc être fait en lien étroit avec l'analyse des dangers.
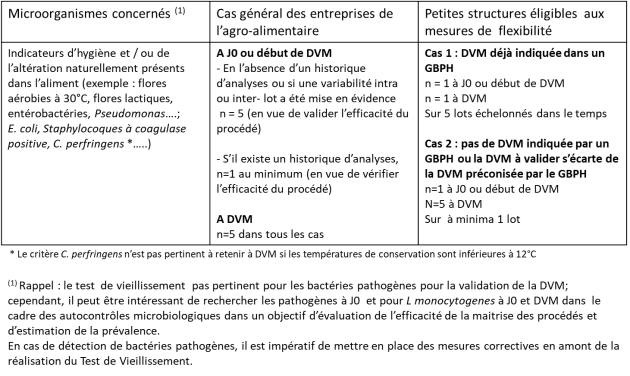
Un exemple de plan d'échantillonnage pour la réalisation des tests de vieillissement en vue de la validation de la DVM est donné ci-dessous :
Conseil :
11 Test de vieillissement microbiologique (norme NF V01-002) : "étude de l’évolution dans un aliment de populations de micro- organismes qui y sont habituellement présents, de façon détectable ou non".
12 Norme NF V01-003 2018 : Traçabilité et sécurité des aliments – Management de l’hygiène – Lignes directrices pour la réalisation de tests de vieillissement microbiologique – Aliments périssables réfrigérés.
c) Cas particulier de Listeria monocytogenes⚓
Pour les aliments prêts à consommer ne permettant pas la croissance de Listeria monocytogenes de par leurs caractéristiques physico-chimiques (cf. Reg CE 2073/2005 : pH ≤ 4,4 ou aw ≤ 0,92 ou pH ≤ 5,0 et aw ≤ 0,94) ou leurs conditions de conservation (produits surgelés ou congelés ou produits réfrigérés à durée de conservation inférieure à 5 jours) ou d'autres paramètres (sous réserve d'une justification scientifique), le critère de 100 ufc/g s'applique pour les produits mis sur le marché pendant leur durée de conservation.
Ainsi, considérant l'absence de croissance de Listeria monocytogenes, la recherche et/ou le dénombrement de Listeria monocytogenes doivent être réalisés à J0 dans l'objectif d'évaluer le niveau de maîtrise du procédé de fabrication, tout en ayant la possibilité de mettre en œuvre des mesures de gestion en cas de résultat non-conforme.
Toutefois, pour les produits entrant dans la catégorie « ne permettant pas la croissance de Listeria monocytogenes » sur la base d'une justification scientifique, il peut être nécessaire de réaliser, en complément, des tests de vieillissement prenant en compte la variabilité inter-lots, et ce, afin de consolider le classement de la denrée dans cette catégorie sur la base également d'un historique de résultats de tests de vieillissement conformes.
Remarque : NB⚓
Pour cette catégorie d'aliments ne permettant pas la croissance de Listeria monocytogenes, le professionnel doit suivre avec pertinence les paramètres physico-chimiques permettant de s'assurer de la maîtrise du process (ex : aw, pH...) ou les autres mesures (exemple : concentration en conservateur) permettant de s'assurer de la maîtrise du process ou de la recette.
Il est à noter également que, malgré l'absence de croissance de Listeria monocytogenes, le professionnel doit mettre en œuvre toutes les mesures de maîtrise visant à prévenir ces contaminations.
Pour les aliments prêts à consommer permettant la croissance de Listeria monocytogenes, deux critères sont définis dans le Reg CE 2073/2005 :
« absence dans 25 g » en fin de production, critère appliqué dans le cas général, notamment lors de la première validation de la DVM d'un produit.
Dans ce cas, la recherche de Listeria monocytogenes doit être réalisée à J0 uniquement et ne sert pas à la détermination initiale de la DVM.
« ≤ 100 ufc/g pour les produits mis sur le marché pendant leur durée de conservation » et susceptibles de présenter un risque de contamination à la sortie de l'établissement de production.
Ce critère permet d'accepter la mise sur le marché de lots pour lesquels l'opérateur a défini un critère intermédiaire en fin de production en cas de présence de Listeria monocytogenes/25g.
Ce critère, à valider par l'opérateur, est en règle générale < 10 ufc/g ou à un seuil de détection inférieur à ce dernier avec une prévalence maîtrisée dans l'atelier de production), et ce, dès lors que le professionnel peut justifier que le seuil de 100 ufc/g sera respecté jusqu'à la fin de la DVM.
La validation de l'application d'un tel critère intermédiaire nécessite néanmoins la constitution d'un dossier, soumis à l'approbation des services d'inspection, comprenant :
- un historique de tests de vieillissement (ces tests seront d'autant plus pertinents qu'ils auront été réalisés sur des lots identifiés à J0 comme étant contaminés en Listeria monocytogenes). L'ensemble de ces résultats permettra de mieux évaluer le pourcentage d'unités susceptibles de dépasser le critère en fin de DVM, et, sous réserve de résultats favorables, d'augmenter le niveau de confiance dans l'évaluation de la maîtrise du process. Les résultats des tests de vieillissement obtenus simplement au stade de la validation initiale ne peuvent pas être jugés suffisants du fait de la faible prévalence de ce pathogène et doivent donc être complétés par des tests de vieillissement supplémentaires dans le cadre de la vérification ;
- et des études complémentaires (cf paragraphe V-B-5).
Dans l'attente de la constitution de ce dossier et de la démonstration du respect de la limite de 100 ufc/g pendant toute la durée de conservation, le critère applicable est « absence dans 25 g » en sortie de l'établissement.
1.5 - Études complémentaires⚓
Des études complémentaires s'avèrent indispensables pour justifier notamment du non-dépassement du critère de 100 ufc/g en Listeria monocytogenes pendant toute la durée de conservation dans les denrées prêtes à être consommées permettant la croissance de Listeria monocytogenes. En effet, bien qu'un historique de résultats de tests de vieillissement soit essentiel car représentatif de la variabilité des conditions de fabrication pour des produits identiques, fabriqués selon le même procédé, le nombre de données collectées demeure usuellement insuffisant pour permettre d'évaluer le comportement de Listeria monocytogenes au cours de la durée de vie, dans le cas d'une faible contamination à Je (la faible prévalence ne permet pas de disposer d'un nombre important d'analyses pour lesquelles le produit est contaminé dès Je et donc de démontrer le respect du critère en fin de durée de vie).
Les outils complémentaires tels que les tests de croissance et/ou la microbiologie prévisionnelle permettent ainsi, sous réserve de la concordance de l'ensemble des résultats14, de consolider les informations conférées par l'exploitation d'un historique de résultats de tests de vieillissement.
Il est à noter que ces outils complémentaires peuvent être utiles pour évaluer l'évolution du comportement d'autres micro-organismes que Listeria monocytogenes, et notamment ceux pour lesquels il existe des critères quantitatifs tels que Staphylococcus à coagulase positive, Bacillus cereus, etc.
a) Tests de croissance⚓
Les tests de croissance 15 ont pour objectif de fournir une information sur le comportement des micro- organismes inoculés artificiellement dans un aliment avant son stockage sous différentes conditions. Ces tests peuvent être utilisés pour :
déterminer le potentiel de croissance, c'est-à-dire savoir si un micro-organisme peut se développer dans un aliment au cours de sa durée de vie et, le cas échéant, connaître l'amplitude de sa croissance,
ou évaluer le taux de croissance, c'est-à-dire la vitesse de multiplication, utile en particulier dans un objectif de microbiologie prévisionnelle (par exemple, prise en compte des variabilités physico- chimiques et scénarii de température).
Le choix du test dépend de l'objectif de l'opérateur. L'annexe Il précise les différences entre les tests permettant de déterminer le potentiel de croissance et ceux permettant d'évaluer le taux de croissance et, dans chacun des cas, les informations qu'ils apportent aux professionnels et aux services de contrôle.
Les tests de croissance doivent prendre en compte la variabilité des caractéristiques physico-chimiques et biologiques des aliments, la contamination spécifique des produits (choix des souches selon des critères techniques), même si le niveau de contamination, son hétérogénéité et l'état physiologique des micro-
organismes dans des conditions naturelles (stress induit par les étapes du procédé de fabrication) sont difficiles à reproduire. Il convient de s'assurer de la pertinence du protocole appliqué et des modalités d'interprétation mises en œuvre.
La norme NF EN ISO 20976-1:2019'6 doit être appliquée pour la conduite de tests de croissance. Dans le cas des tests relatifs à L. monocytogenes, le guide technique LRUE Lm, complémentaire à cette norme, doit également être suivi (voir note bas de page 13 pour le lien).
Pour les tests relatifs à Listeria monocytogenes, un réseau de laboratoires reconnus, supervisé par le Laboratoire National de Référence de l'Anses (LNR), a été mis en place par la DGAL afin d'apporter les garanties suffisantes aux services officiels pour la vérification des résultats analytiques des études de durée de vie. L'ensemble des exigences techniques et des compétences requises pour ces laboratoires est décrit dans l'instruction DGAL/SDPAL/2016-688 du 25 août 2016.
La Iiste des laboratoires reconnus est accessible sur le site du ministère http:||agricuIture.gouv.fr/laboratoires-agrees-et-reconnus-methodes-officielles-en-alimentation.
Seuls les laboratoires figurant sur cette Iiste peuvent réaliser les tests de croissance de Listeria monocytogenes dans les denrées alimentaires en application de l'article 3 du Reg CE 2073/2005.
Note : la mise en œuvre d'un test de croissance n'est souvent pas pertinente si des données démontrent que le micro-organisme considéré se développe de façon rapide dans un aliment similaire. Ces tests sont surtout intéressants pour évaluer le comportement d'un micro-organisme identifié Iors de l'analyse des dangers microbiologiques ou pour une bactérie pathogène (critère de sécurité) difficile à détecter Iors des analyses d'auto-contrôles : c'est le cas lors de la création d'une nouvelle recette, pour un aliment qui, du fait de ses caractéristiques physico-chimiques, se situe à la frontière entre croissance et non-croissance (la prise en compte de la variabilité des fabrications est alors essentielle) ou lorsque l'on suspecte que la croissance du micro-organisme étudié est lente. |
b) Microbiologie prévisionnelle⚓
La microbiologie prévisionnelle est la discipline permettant de prédire, à l'aide de modèles mathématiques, le comportement d'un micro-organisme donné dans un aliment donné, en fonction de ses caractéristiques physico-chimiques et des conditions de conservation ou des traitements qu'il subit (température, aw, pH...). La microbiologie prévisionnelle permet en outre de tenir compte des données issues des résultats d'autocontrôle microbiologique sur la prévalence et la quantification du microorganisme dans d'aliment. La microbiologie prévisionnelle permet ainsi de combiner un niveau de contamination initiale réaliste (généralement faible) à une simulation du comportement microbien.
La pertinence du modèle utilisé doit être justifiée ; l'utilisation de modèles élaborés spécifiquement pour la simulation du comportement microbien dans un aliment similaire doit être privilégiée.
Pour l'utilisation de modèles mathématiques prédictifs, on peut distinguer deux approches :
l'approche déterministe qui permet de simuler le développement microbien et de prédire si le seuil limite fixé est dépassé en fin de durée de vie,
l'approche probabiliste qui permet de prédire une probabilité de dépasser le seuil limite fixé en fin de durée de vie.
L'opérateur mettant en œuvre les modèles doit disposer des compétences nécessaires, ou faire appel à un prestataire qualifié, notamment pour choisir les paramètres d'entrée du modèle (caractéristiques de l'aliment et du micro-organisme), tenir compte des incertitudes autour des données et interpréter avec précision les résultats de l'une ou l'autre approche.
Il est demandé à l'utilisateur de fournir un compte-rendu de la simulation comportant la description du modèle utilisé, la démarche d'estimation des valeurs des paramètres, le résultat des simulations, la démarche de prise en compte de la variabilité et de l'incertitude. Tous les enregistrements doivent être conservés.
Des informations complémentaires sur le sujet sont disponibles auprès du réseau mixte technologique (RMT) ACTIA QuaIima 17 et notamment, deux notes sur des lignes directrices d'aide à l'utilisation des outils de microbiologie prévisionnelle et à l'interprétation des résultats et sur l'appréciation quantitative de l'exposition et/ou des risques.
Conseil :
14 Plusieurs études menées sur la filière saumons et truites fumés indiquent, qu‘en ne tenant pas compte du stress des souches lié au process, les résultats des tests de vieillissement et de la modélisation par microbiologie prévisionnelle peuvent surestimer la croissance de Listeria monocytogenes. L'organisation professionnelle représentative de cette filière (la CITPPM) travaille sur ce sujet depuis plusieurs années et a développé en 2023 une méthode normalisée NF V45-009 permettant de quantifier des teneurs en Listeria mononocytogenes à partir de 1 UFC/g afin d'affiner au mieux la gestion du risque Lm dans ce contexte. Par ailleurs, une thèse a démarré en 2024 sur la prise en compte du stress des souches sur la croissance de Lm dans le saumon fumé.
15 Test de croissance (norme NF EN ISO 20976-1 : 2019): "étude de l'évolution de la population de micro-organismes ajoutés dans un aliment, comportant le dénombrement de la population initiale ajoutée". Note : les tests de croissance sont utilisés plus particulièrement lorsque l'on étudie des micro-organismes pathogènes qui ne sont pas détectables de façon habituelle dans l'aliment. D‘autres espèces microbiennes d'intérêt peuvent être étudiées dans le cas d'une optimisation de recette, par exemple.
16 Norme NF EN ISO 20976:2019 : Microbiologie de la chaîne alimentaire — Exigences et lignes directrices pour la réalisation des tests d'épreuve microbiologique — Partie 1 : Tests de croissance pour étudier le potentiel de croissance, le temps de latence et le taux de croissance maximal.
17 Ce réseau national, mis en place et soutenu par le MAA, sous la coordination de l'ACTIA, organisme porteur AERIAL co-animé avec ACTALIA, est dédié à la maîtrise de la qualité microbiologique des aliments. Il regroupe 19 partenaires (six ITAI, organismes publics dont la DGAL, l'Anses, centres de recherche & enseignement, centre technique C NIEL). Qualima a pour objectif de développer des travaux pour une alimentation microbiologiquement sûre et saine, dans un contexte d'évolution des attentes sociétales. Les acteurs permettent une approche pluridisciplinaire en microbiologie et en physico-chimie des aliments, en génie des procédés alimentaires & frigorifiques et modélisation/biostatistiques, et en appréciation quantitative de l'exposition et du risque microbiologique. Pour en savoir plus: https’//www actia-asso eu/projets/quaIima-2/
1.6 - Cas particulier de Listeria monocytogenes⚓
Note : Afin de déterminer si une denrée doit être considérée comme une denrée prête à consommer, il convient de se référer à l'instruction technique DGAL/SDSSA 2023-27 relative aux dispositions réglementaires au regard du danger Listeria monocytogenes applicables à la production et la mise sur le marché de denrées d'origine animale ou en contenant prêtes à être consommées. |
a) Aliments prêts à consommer ne permettant pas la croissance de Listeria monocytogenes
Pour les aliments prêts à consommer ne permettant pas la croissance de Listeria monocytogenes de par Ieurs caractéristiques physico-chimiques (cf. Reg CE 2073/2005 : pH <=4,4 ou aw <= 0,92 ou pH <= 5,0 et aw< 0,94) ou Ieurs conditions de conservation (produits surgelés ou congelés ou produits réfrigérés à durée de conservation inférieure à 5 jours) ou d'autres paramètres (sous réserve d'une justification scientifique telles que, par exemple, la littérature scientifique, la microbiologie prévisionnelle, le test de croissance), le critère de 100 ufc/g s'applique pour les produits mis sur le marché pendant Ieur durée de conservation. Ainsi, considérant l'absence de croissance de Listeria monocytogenes, la recherche et/ou le dénombrement de Listeria monocytogenes doivent être réalisés à Je dans l'objectif d'évaluer le niveau de maîtrise du procédé de fabrication, tout en ayant la possibilité de mettre en œuvre des mesures de gestion en cas de résultat non- conforme.
Toutefois, pour les produits entrant dans la catégorie « ne permettant pas la croissance de Listeria monocytogenes » sur la base d'une justification scientifique, il peut être nécessaire de réaliser, en complément, des tests de vieillissement prenant en compte la variabilité inter-lots, et ce, afin de consolider le classement de la denrée dans cette catégorie sur la base également d'un historique de résultats de tests de vieillissement conformes.
En complément, un test de croissance déterminant le potentiel de croissance peut être réalisé pour justifier cette non-croissance et classifier le produit dans la catégorie 1.3 du Reg CE 2073/2005 (produit nepermettant pas le développement de L. monocytogenes). Depuis avril 2019, le protocole à suivre pour déterminer ce potentiel est celui de la norme NF EN ISO 20976-1 qui diffère de référentiels précédents, tels que la norme NF V 01-009 et la version 43 du Guide Technique du LRUE Lm. Cette modification pouvant conduire à des interprétations différentes, il est important de connaitre la date à laquelle ce test a été réalisé.
Le test de croissance est notamment utile pour les aliments dont les caractéristiques physicochimiques sont à l'interface croissance / non-croissance ou pour les aliments avec des conservateurs ou des effets barrière.
Note : pour cette catégorie d'aliments ne permettant pas la croissance de Listeria monocytogenes, le professionnel doit suivre avec pertinence les paramètres physico-chimiques permettant de s'assurer de la maîtrise du process (ex : aw, pH...) ou les autres mesures (exemple : concentration en conservateur, présence d'une flore technologique ou de biopréservation) permettant de s'assurer de la maîtrise du process ou de la recette. La caractérisation de la variabilité physico-chimique pour s'assurer de la non-croissance est indispensable. |
Il est à noter également que, malgré l'absence de croissance de Listeria monocytogenes, le professionnel doit mettre en œuvre toutes les mesures de maîtrise visant à prévenir ces contaminations.
b) Aliments prêts à consommer permettant la croissance de Listeria monocytogenes
Pour les aliments prêts à consommer permettant la croissance de Listeria monocytogenes,deux critères sont définis dans le Reg CE 2073/2005
« Non détecté dans 25 g » avant que la denrée alimentaire n'ait quitté le contrôle immédiat de l'opérateur qui l'a fabriquée, critère appliqué dans le cas général, notamment Iors de la première validation de la DVM d'un produit. Dans ce cas, la recherche de Listeria monocytogenes doit être réalisée à Je uniquement et ne sert pas à la détermination initiale de la DVM.
« <=100 ufc/g pour les produits mis sur le marché pendant leur durée de conservation » et susceptibles de présenter un risque de contamination à la sortie de l'établissement de production. Ce critère permet d'accepter la mise sur le marché de lots pour lesquels l'opérateur a défini un critère intermédiaire en fin de production en cas de présence de Listeria monocytogenes/25g. Ce critère intermédiaire, à valider par l'opérateur, est en règle générale < 10 ufc/g ou à un seuil de détection inférieur à ce dernier avec une prévalence maîtrisée dans l'atelier de production, et ce, dès Iors que le professionnel peut justifier que le seuil de 100 ufc/g sera respecté jusqu'à la fin de la DLC.
La validation de l'application d'un tel critère intermédiaire nécessite néanmoins la constitution d'un dossier, soumis à l'examen des services d'inspection, comprenant :
un historique de tests de vieillissement (ces tests seront d'autant plus pertinents qu'ils auront été réalisés sur des lots identifiés à Je comme étant contaminés en Listeria monocytogenes). L'ensemble de ces résultats permettra de mieux évaluer le pourcentage d'unités susceptibles de dépasser le critère en fin de DLC, et, sous réserve de résultats favorables, d'augmenter le niveau de confiance dans l'évaluation de la maîtrise du process.
Remarque : les résultats des tests de vieillissement obtenus simplement au stade de la validation initiale ne peuvent pas être jugés suffisants du (ait de la faible prévalence de ce pathogène et doivent donc être complétés par des tests de vieillissement supplémentaires dans le cadre de la vérification.
et des études complémentaires (cf paragraphe II.1.5).
Dans l'attente de la constitution de ce dossier et de la démonstration à la satisfaction de l'autorité compétente du respect de la limite de 100 ufc/g pendant toute la durée de conservation, le critère applicable est « non détecté dans 25 g » en sortie de l'établissement. |
1.7 - Nouvelle validation de DVM⚓
La durée de vie microbiologique des denrées peut nécessiter, le cas échéant, une nouvelle validation dans les cas suivants :
tout changement significatif dans la composition de produits existants (ingrédients, additifs, etc.),
modifications de l'atelier de fabrication et/ou des équipements de production.
développement de produits nouveaux ou modification de produits existants,
développement de nouveaux procédés de fabrication ou modification de procédés existants,
utilisation de nouveaux types de conditionnement ou modification de conditionnements existants.